
(特约通讯员:胡瑞年 报道)“防治肥胖,势在必行”。近日,武昌理工学院生命科学学院朱琳老师参与的团队在《Food & Function》杂志上发表了最新研究成果Structural characterization of Poria cocos oligosaccharides and their effects on the hepatic metabolome in high-fat diet-fed mice。在该研究中,我们首次从茯苓多糖中提取茯苓寡糖(PCO),并通过HPLC、GC-MS、FT-IR、NMR光谱等技术对其结构特征进行了分析鉴定。使用高脂饮食(HFD)喂养的血脂异常小鼠模型,通过非靶向代谢组学技术进一步证实PCO可以显著抑制血液和肝脏组织中的脂质积累和炎症反应。该研究揭示了PCO在治疗血脂异常方面的潜在应用。
通过HPLC、LC-MS、PMP单糖衍生和FT-IR分析,初步确定PCO是一种单糖组成为甘露糖、葡萄糖、半乳糖和阿拉伯糖,聚合度为2-6的寡糖成分(图1)。除此之外,我们还进行了甲基化分析和核磁共振分析进一步对PCO的结构进行表征。
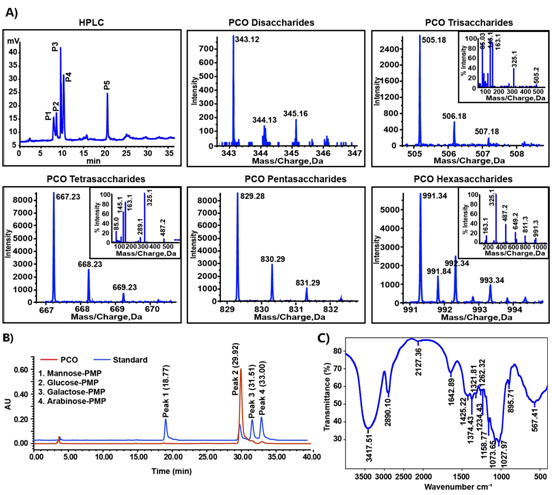
图1 PCO的结构分析
基于高脂饮食(HFD)诱导的肥胖小鼠模型,我们进一步探究了PCO对于糖脂代谢紊乱的调节作用。其结果表明,PCO不仅能够有效降低高脂饮食导致的高血脂水平,同时能够调控糖脂代谢相关基因水平和逆转炎症因子的高表达,从而预防肝脏组织中脂滴的沉积和炎症细胞的浸润(图2)。
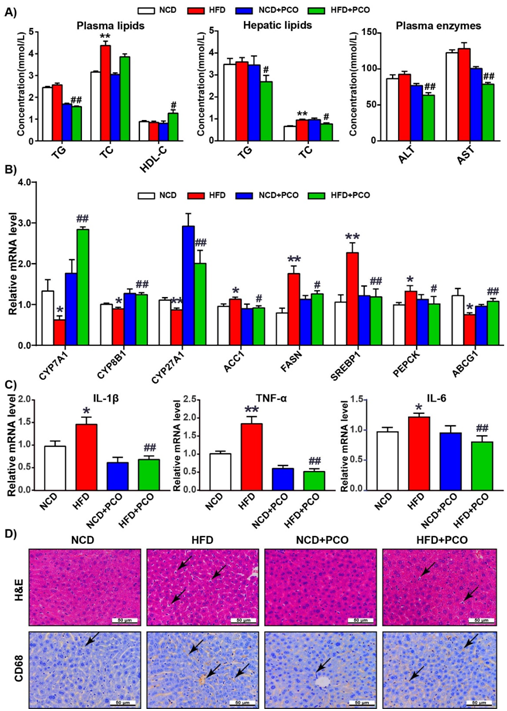
图2 PCO抑制高脂饮食小鼠糖脂代谢紊乱及炎症聚集
通过对小鼠肝脏组织进行非靶向代谢组学分析,进一步证实PCO可能通过调控甘油磷脂代谢、脂肪酸代谢、胆汁酸代谢、色氨酸代谢和鞘脂代谢等代谢通路对抗高脂饮食诱导的血脂异常(图3)。
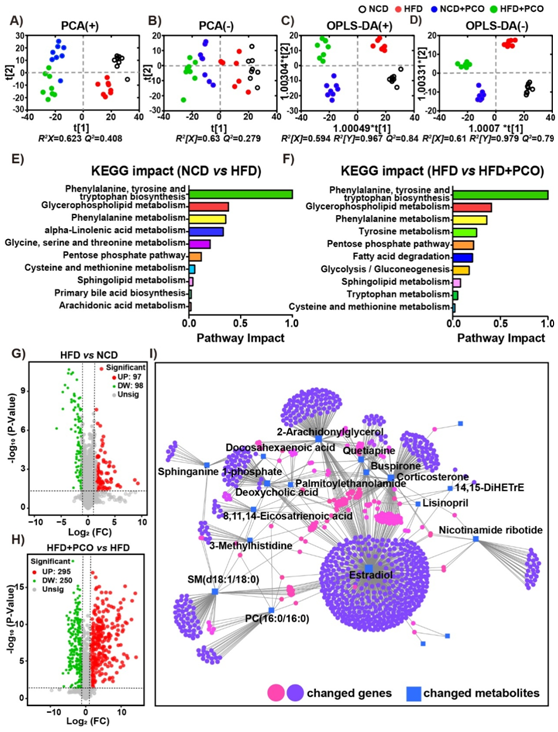
图3 基于肝脏组织代谢组学的代谢物聚类、显著变化的KEGG通路和相关基因-代谢物网络图
据悉,本课题首次提取茯苓寡糖(PCO)并对其进行结构表征,并初步证实PCO作为益生元在治疗肥胖相关的血脂异常的潜力,为未来肥胖相关疾病的防治提供了新的策略,也为肥胖相关人群的健康与护理提供了福音。(完)